小野俊介准教授による分析
以下、東京大学医薬品評価学講座の小野俊介准教授による原因分析を紹介する。
素人の偏見への批判
薬の問題の難しさ
- たくさんの登場人物。
- 誰が味方で、誰が敵かがはっきりしない。
- 八つ当たりするのにちょうどいい相手が霞ヶ関や虎ノ門あたりにいるのが、不幸の源。
- 八つ当たりですっきりしても、実は何も解決しないから。
ステレオタイプな主張はもうやめましょう
成果を出すための政策の立案・実施の妨げになっています
- 「ドラッグラグ問題が近年深刻化している。」
- 「近年」「どの程度深刻化」は誰も確かめていない。
- 「国内治験数の減少は、日本の治験が高コストでスピードが遅いからだ。」
- 生産者の側に思い入れがあり過ぎ。建設業好きの日本人ならでは。
- 「ドラッグラグは国内治験体制が欧米に劣っているから生じる。」
- 何がどう劣っているのか、まともな説明を聴いたことは一度もない。
- 劣っている「から」かどうか誰も確かめていない。
- 「ドラッグラグ解決のカギは国際共同治験だ。」
- 「少子化解決のカギは夫婦のベッドルームの改善だ」くらいの信頼度。
- 「当局の審査員を増やせば新薬の審査時間は短くなるはず。」
- 審査時間が短縮する保証はない(後述)。
「ドラッグラグは企業の効率の証」でもある
- 製薬企業が効率的だから、ドラッグラグが生じる。
- 「ドラッグラグをなくす」とは、どこかに歪み・非効率をもたらすこと。
- 企業をぶん殴ってドラッグラグを短期的になくすことと、長期的に日本の患者が幸せになることは、一致しない。
- 「企業には日本で早くお薬を供給する社会的責任があるはずだ。」
- 他人を不愉快にするだけの台詞。
- 「では企業任せにせずに、国が新薬の研究開発を主導すべきだ。」
- そんなバカげた発想は捨てるべきです。お金をドブに捨てるのと同義です。
結論:ステレオタイプな主張を見分けましょう
- ある米国人:「日本のようなGDP世界第二位の大国が、なぜワクチンプログラムを持っていないのか、不思議でならない。」
- 私:「米国のようなGDP世界第一位の超大国が、なぜ国民皆保険を持っていないのか、不思議でならない。」←これもステレオタイプ。
- 参考: 各国のホームレスの数(生田武志.ルポ最底辺(ちくま新書))
- 日本:約3万人(2007)。増加中
- 大本営発表は、1万9千人(2007)。厚労省はホームレスがどこにいるかを把握していないため。
- 米:350万人(うち子供が135万人(2004))
- 英:10万家族(2006)
- 仏:20万人(2002)
- 中国:約67万人(2003.8-2004.11)
医療問題に限らず、何か批判するときに、企業の利潤追求はケシカランとか、行政が国民の利益を全く考えてないとか、そうしたステレオタイプの批判は結構多い。 しかし、そうしたステレオタイプの批判は、大抵、偏見に基づいていることが多い。 (←ステレオタイプは偏見の一種だから、この文章は日本語としておかしい。)
製薬会社の利潤追求は、医薬品等の開発の原動力となるものである。 企業の利潤追求を批判することは、企業のやる気を削げと言うに等しい。 企業がやる気を失っても上手くいくと考えるのは、楽観的な理想主義であり、非現実的な共産主義的な発想である。 国が研究開発を主導すれば、経済的な効率が置き去りになって、結果として費用対効果は下がり、国民にとって損になる。 少ない負担で国民が幸福になるには、企業の利潤追求を原動力として上手く利用する必要があるのだ。 企業の利潤追求と国民の幸福の利害が一致するよう国の制度を整備すれば良いのであって、利潤追求を批判するのは見当違いである。
行政が国民の利益を全く考えてない、そう主張する人は、行政について何も勉強していないことが多い。 行政が何を考えて何を目指しているのか、それを学べば、行政が国民の利益を目的として行動していることが分かる。 行政の認識が世間離れしてることもあるが、その原因は国民とのパイプが細いからに他ならない。 行政と国民の間にしっかりとしたパイプを築けば、行政はちゃんと国民のための仕事をしてくれるのである。 そして、そのためには、国民の側から働きかけなければならないのである。 何故なら、世間離れした行政は、問題があることを認識していないからである。
小野俊介准教授が指摘する「ステレオタイプな主張」の多くは、そうした偏見から発生している。 (←ステレオタイプは偏見の一種だから、この文章は日本語としておかしい。) そうした偏見を排除し、キチンと事実関係を調べることが重要である。
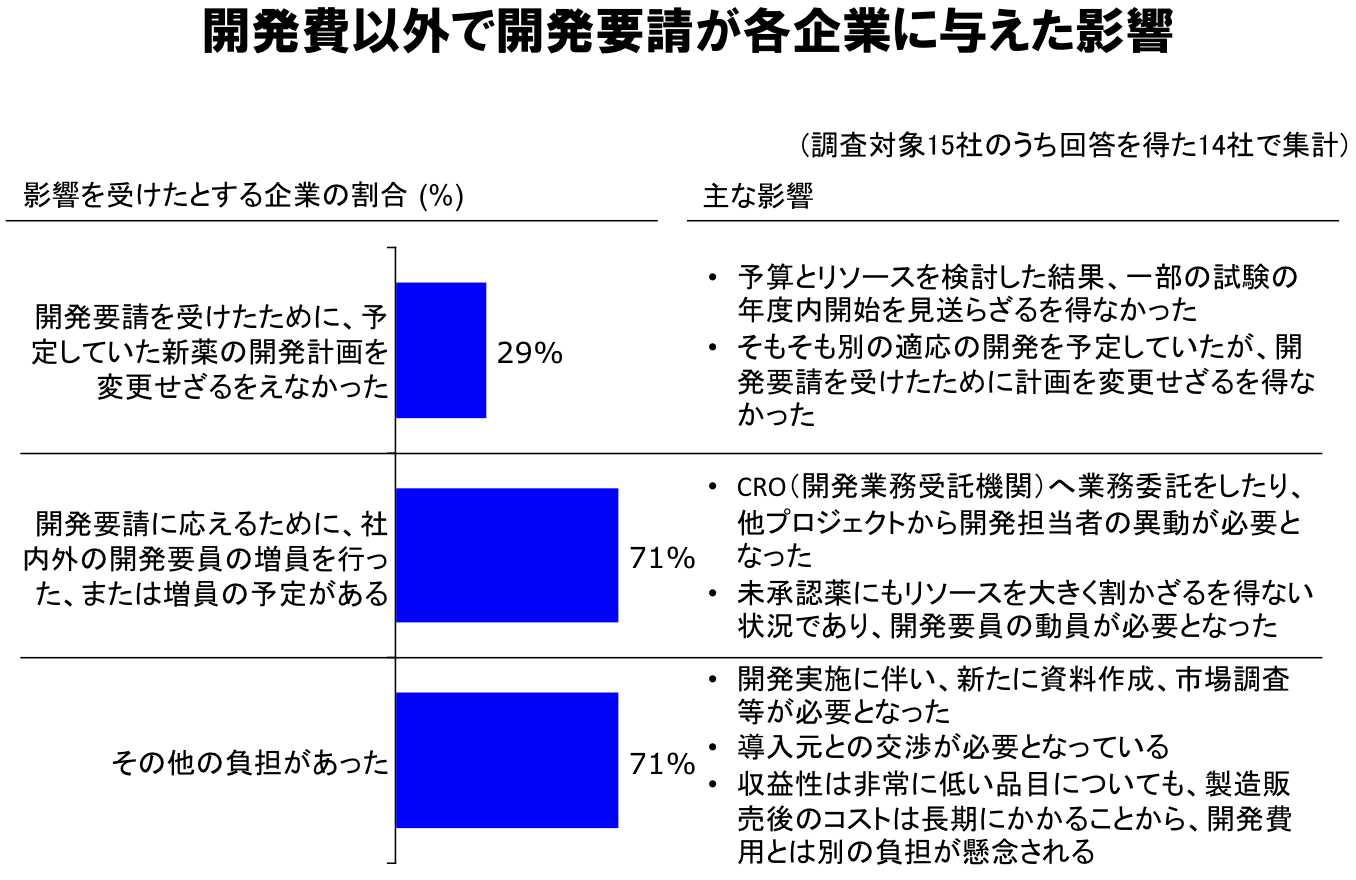
企業は儲かる所に集中的に投資する。 その結果、儲からない所は後回しにされるか完全にスルーされる。 日本の医薬品市場は企業にとって儲からないから、後回しにされるか完全にスルーされる。 「ドラッグラグは企業の効率の証」だからこそ、このようなことが起こるのである。 だったら、日本の医薬品市場で企業が適正に儲けられるようにすればいい。 「企業をぶん殴ってドラッグラグを短期的になくすこと」が「どこかに歪み・非効率をもたらす」ことになり「長期的に日本の患者が幸せになることは、一致しない」実例を1つ挙げる。 2010年より新薬創出・適応外薬解消等促進加算制度が試行された。 この制度では、国が要請した医薬品開発に応じた製薬会社には、新薬の価格維持のインセンティブが与えられる。 その一方で、国が要請した医薬品開発に応じない製薬会社には、そうしたインセンティブは与えられない。 この制度で製薬会社が国の要請に応じることによって、他の新薬の開発計画に影響を与えている。
「開発要請を受けたために、予定していた新薬の開発計画を変更せざるをえなかった」「一部の試験の年度内開始を見送らざるを得なかった」を見れば、国の要請が別の薬ドラッグラグ・未承認薬問題の原因になっていることが分かる。 やはり、「企業をぶん殴ってドラッグラグを短期的になくす」のではなく、製薬会社が心から開発したくなるような制度が必要だろう。
日本の国際競争力が弱い原因
「ステレオタイプな主張」に対する最も衝撃的な批判がこれであろう。
日本企業・アカデミアの国際競争力が弱いのは当然
・・・当局の審査力が弱いことより、こちらははるかに深刻
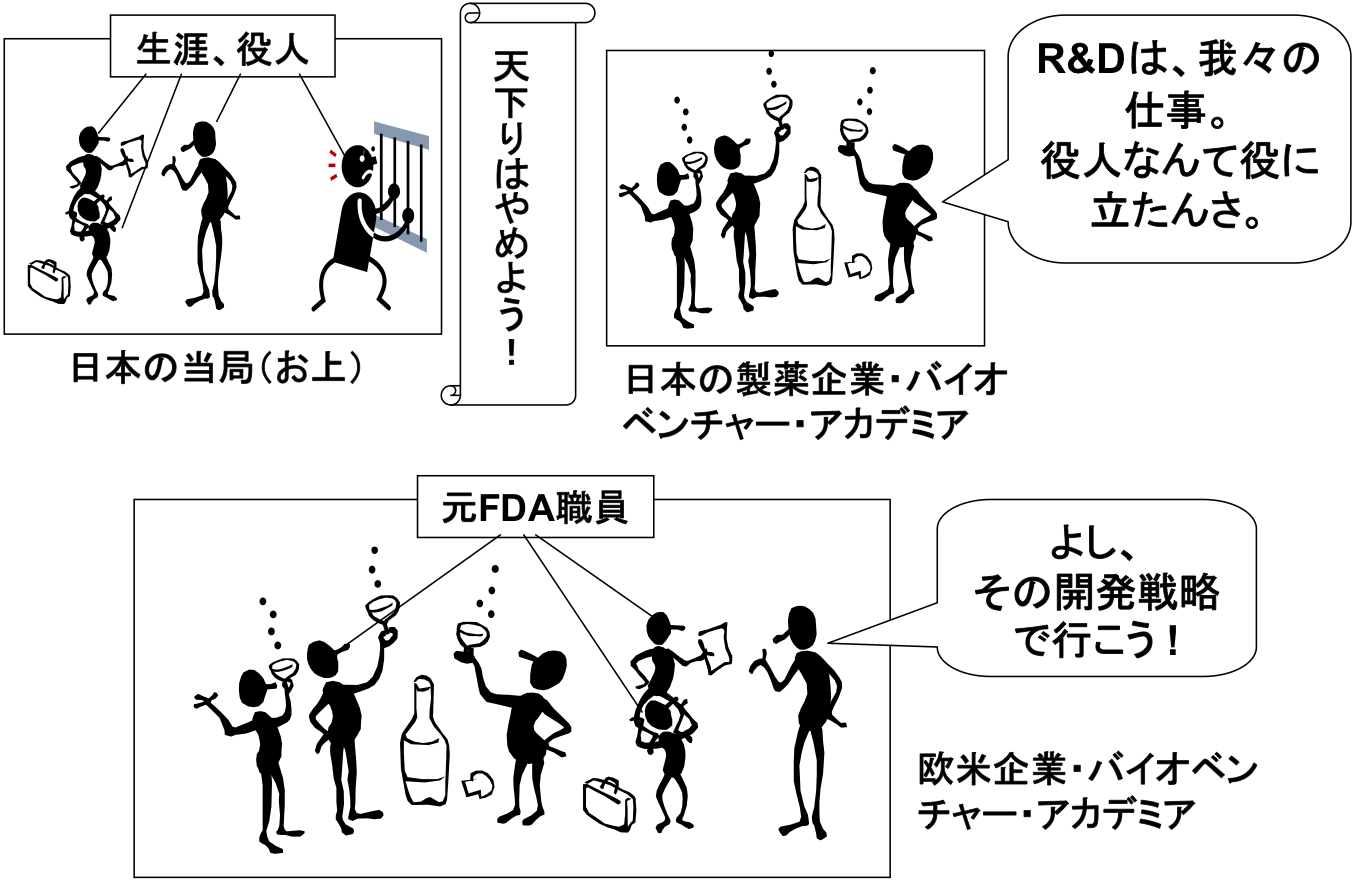
ようするに、天下りを禁止することが新薬開発においてマイナスになると指摘しているのである。 一般に天下りは、国民の血税の使途の不公平さと無駄使いの観点から悪いことだと言われている。 確かに、その指摘は一利ある。 しかし、天下りによって新薬の開発が著しく改善され、その結果、多くの国民の命を救えるなら、天下りの欠点など大した問題ではなかろう。 国民にとって大きな利益である新薬の充実を捨ててまで、瑣細な問題に目くじらを立てるのは本末転倒ではないか。 …と小野俊介准教授は批判しているのだろう。 と、ここは小野俊介准教授のせいにして逃げておく(笑)。
治験を増やすには
日本での治験数減少の理由
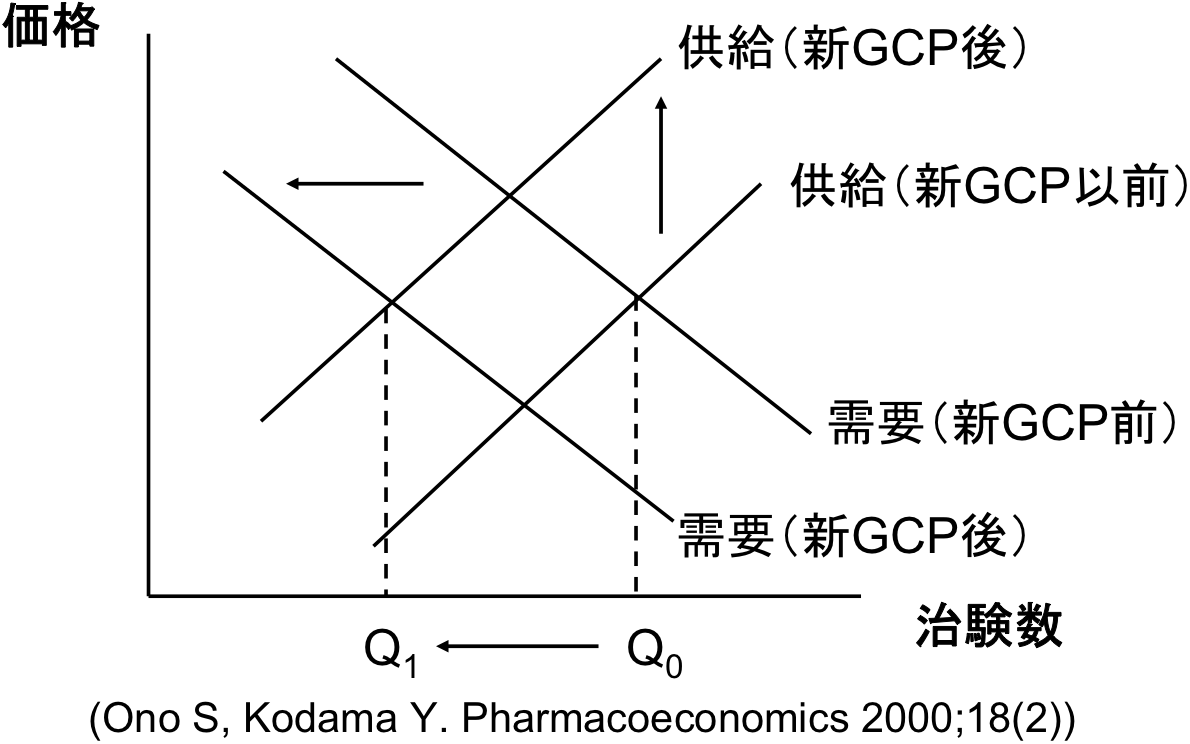
<重要>治験の数は、需要と供給で決まる
- 治験の需要者:製薬企業(承認申請用に提出するため)
- 治験の供給者:治験実施施設
日本の治験数に影響を与える要因
- 被験者となるべき者に対する治験に関する文書による説明と同意の取得
- 治験総括医師制度の廃止
- 治験依頼者の責任範囲の拡大と強化
- 業務手順書、治験実施計画書、治験薬概要書等の作成義務
- モニタリング・監査等の治験管理の実施
- 治験総括報告書の作成
- 治験審査委員会の機能の充実
- 外部委員、非専門家委員の参加の義務付け
- 審査機能、責務の明確化
- 治験責任医師の責任と業務の明確化
- 医療機関における治験事務局の強化
全体的に基準が厳しくなったように見える。 だとすると、治験の供給者としては、治験の価格を高くしたいと思うだろう。 一方、治験の需要者としては、治験の管理にかかるコストが増えるならば、治験そのものの価格を低くしたいと思うだろう。 結果として、小野俊介准教授の指摘の通り、需要曲線と供給曲線は移動し、治験数が減少することになる。
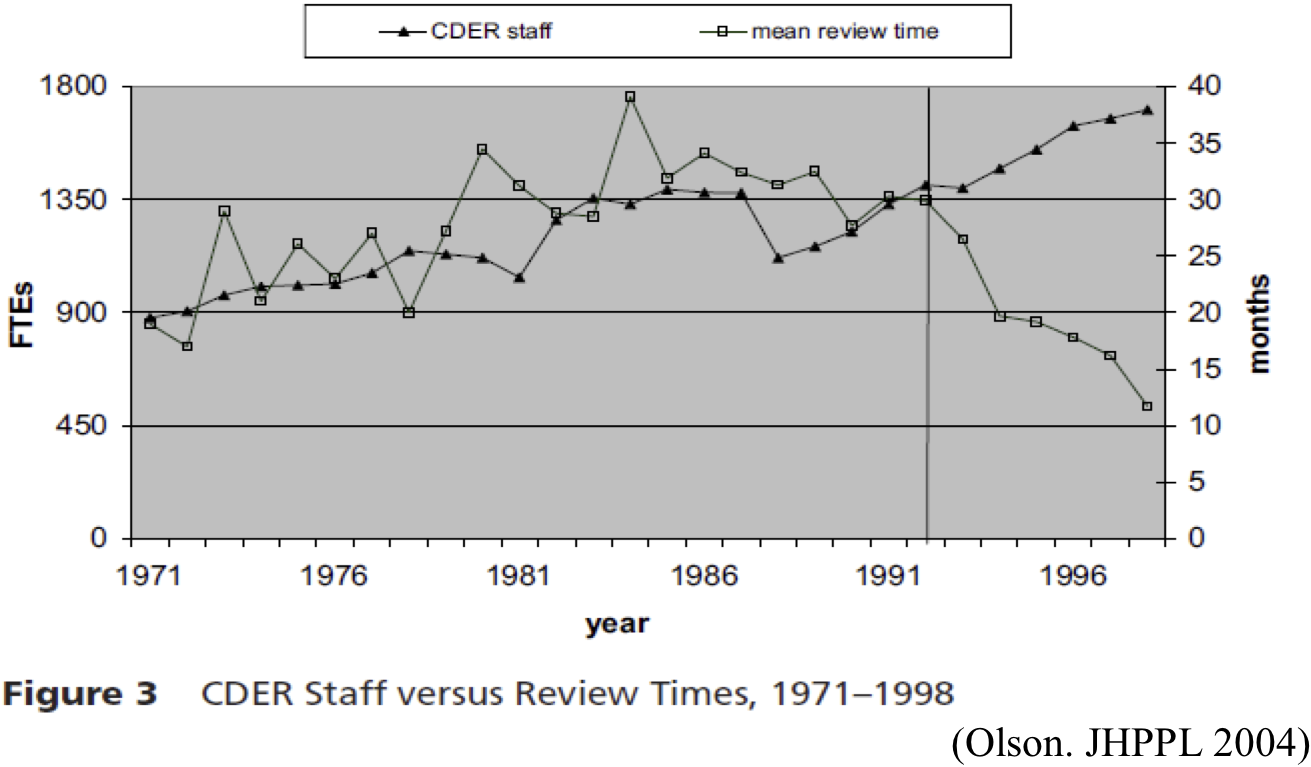
米国の承認審査時間とマンパワーの関係
- ポイント1: 審査時間が激減したのは、ユーザーフィー法の成立後。
- (審査員の数と審査期間との関係はそう単純ではない。)
- ポイント2: このグラフが、日本の議論で出たことはない。
米国の承認審査を劇的に変えたユーザーフィー法のポイント
目が血走りそうな仕組み満載
- 5年ごとに切れるサンセット法。
- 新薬審査に要する人件費等を製薬企業が出す。
- 出してもらった金は新薬審査にしか使えない。
- ある意味、審査官の雇用がかかっている。
- 審査時間等の達成目標を事前に設定。
- 法を延長(更新)するには、5年ごとに米議会の承認が必要(直近の更新は昨年9月)。
- 米議会が目標の達成率を監視。
医薬品評価研究センター(CDER)は米国食品医薬品局(FDA)内の医薬品の審査をする部門である。 1971年から1991年までのグラフを見ると、CDERの要員が増えても審査期間は短くなっていない。 というより、CDERの要員が増えているのに、逆に、審査期間は長くなっている。 ところが、1991年にユーザーフィー法が成立して以降、急激に審査期間が減少している。 以上のことから、「当局の審査員を増やせば新薬の審査時間は短くなるはず」とする主張は正しくない。
日本での治験
「わざわざ日本で試験をやる必要はない」は正しいか
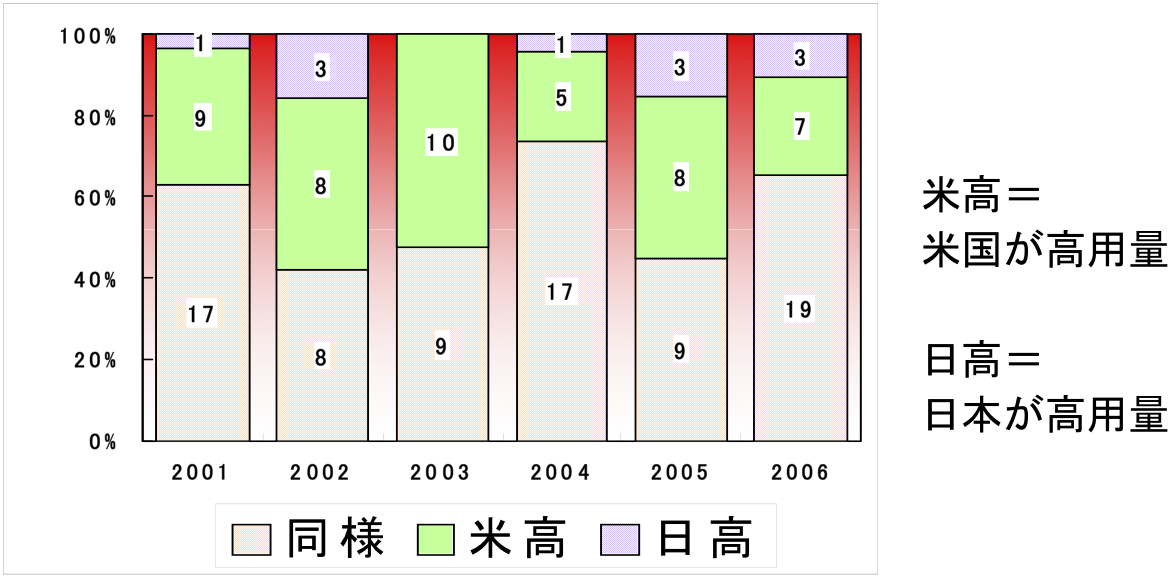
新薬の日米間の用量比較
- ポイント1:製薬企業は臨床試験の結果を踏まえて、新薬を各国仕様にカスタマイズしている。せざるをえない。
- ポイント2:カスタマイズしなかったら?副作用で黄疸が出たり。誰も気づかぬまま、何十年も、少しずつ、死にそうな人や死ぬ人が出る。
欧米で効果が実証されているのだから日本で治験をやるのは無駄だと主張する人がいる。 しかし、小野俊介准教授の指摘によれば、用量決定や副作用に関する治験は必要である。 そして、現在の日本の制度は、用量決定や副作用に関する追加データを用意すれば欧米の治験データが流用できるようになったはずである。
まとめ
小野俊介准教授の指摘をまとめれば、大凡次のようになるのだろう。
- 製薬会社にとって日本の医薬品市場に魅力がない。
- 製薬会社と国の方針がバラバラでチグハグなことをやっている。
- 原因を適切に分析せずに余計なことをすれば返って制度が歪みかねない。
メニュー
素晴らしき国民皆保険制度
医療制度問題
- 混合診療問題に関する誤解
- 混合診療より保険充実がまずありき(MRIC)
- ドラッグラグ・未承認薬の本質と改革案
- 小野俊介准教授による分析
- 使えない承認済医薬品
- 使い難い55年通知(適応外処方)
- 特許制度と医療制度の乖離
- 自由診療の問題
懸念事項
- 混合診療による国民皆保険崩壊の原理
- 混合診療に関わる医療利権
- インチキ療法蔓延の懸念
- 混合診療解禁の必要性はあるか?
それぞれの改革案
マスコミ報道等
- 混合診療社説と言う名のプロパガンダ
- 日本の薬価は高いのか?「薬価の国際比較調査にもとづく医療保険財源提案(薬価の国際比較-2010年薬価の比較調査報告書-)」
- まずは薬価全体を引き上げよ!ニボルマブ(オプジーボ)を下げる前に